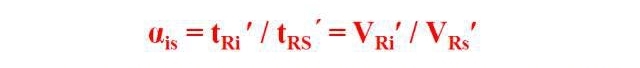kromatografia, "analisi kromatografikoa", "kromatografia" izenez ere ezaguna, bereizketa- eta analisi-metodo bat da, eta aplikazio oso zabala du kimika analitikoan, kimika organikoan, biokimikan eta beste alor batzuetan.
Kromatografiaren sortzailea M.Tsvetter botanikari errusiarra da.1906an, Zvetter botanikari errusiarrak bere esperimentuaren emaitzak argitaratu zituen: Landare-pigmentuak bereizteko, landare-pigmentuak zituen petrolio-eter-estraktua bota zuen kaltzio karbonato hautsa zuen kristalezko hodi batean eta petrolio-eterrez eluatu zuen goitik behera.Pigmentu ezberdinek kaltzio karbonato partikulen gainazalean adsortzio-ahalmen desberdinak dituztenez, lixibiatzeko prozesuarekin, pigmentu desberdinak abiadura ezberdinetan jaisten dira, eta horrela kolore ezberdinetako bandak sortzen dira.Pigmentuaren osagaiak bereizten ziren.Bereizketa metodo honi kromatografia izena jarri zion.
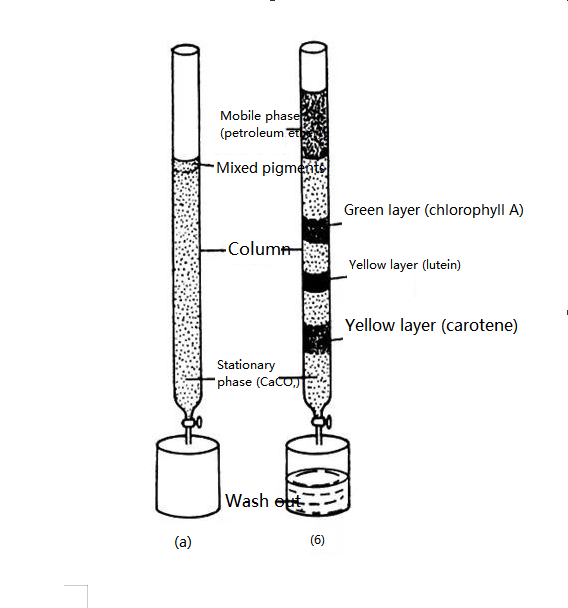
Landareen hostoen pigmentu bereizteko esperimentu baten irudikapen eskematikoa
Bereizketa metodoen etengabeko garapenarekin, gero eta kolorerik gabeko substantzia gehiago bereizteko objektu bihurtzen dira, kromatografiak ere pixkanaka "kolore" esanahia galdu zuen, baina gaur egun oraindik ere izena erabiltzen da.
Sailkapen kromatografikoa
Kromatografiaren funtsa banandu beharreko molekulak fase geldiaren eta fase mugikorren artean banatzen eta orekatzen diren prozesu bat da.Substantzia desberdinak modu ezberdinean banatzen dira bi faseen artean, eta horrek abiadura ezberdinetan mugitzen ditu fase mugikorrarekin.Fase mugikorren mugimenduarekin, nahastearen osagai desberdinak elkarrengandik bereizten dira geldialdian.Mekanismoaren arabera, hainbat kategoriatan bana daiteke.
1, bi faseko egoera fisikoaren sailkapenaren arabera
Fase mugikorra: gas-kromatografia, likido-kromatografia, fluido-kromatografia superkritikoa
Fase geldikoa: gas-solidoa, gas-likidoa;Likido-solido, likido-likido
2, fase geldikorreko sailkapenaren formaren arabera
Zutabe-kromatografia: zutabe-kromatografia paketatua, zutabe kapilar kromatografia, zutabe-kromatografia mikropaketatua, kromatografia prestatzailea
Kromatografia planoa: paperezko kromatografia, geruza meheko kromatografia, polimeroen mintz kromatografia
3, bereizketa mekanismoaren arabera sailkatuta
Adsortzio-kromatografia: osagai desberdinak xurgatzaileetan duten xurgapen- eta desortzio-ahalmenaren arabera bereizten dira.
Parte-kromatografia: osagai desberdinak disolbatzailean duten disolbagarritasunaren arabera bereizten dira
Bazterketa molekularren kromatografia: bereizketaren tamaina molekularraren tamainaren arabera, ioi-trukearen kromatografia: ioi-trukeko erretxina bereizteko afinitatearen osagai desberdinak.
Afinitate-kromatografia: Makromolekula biologikoen arteko afinitate espezifiko baten presentzia erabiliz bereiztea
Elektroforesi kapilarra: osagaiak mugikortasunaren eta/edo partizioaren portaeraren desberdintasunen arabera bereizten ziren
Kromatografia kiral droga kiralak bereizteko eta aztertzeko erabiltzen da, hiru kategoriatan bana daitezkeenak: deribatuzio kiraleko erreaktiboen metodoa;Fase mugikor kiralaren metodo gehigarria;Fase geldikorreko ebazpen-metodoa
Kromatografiarako oinarrizko terminologia
Denboraren aurkako bereizketa kromatografikoa detektatu ondoren osagaien erantzun-seinaleak irudikatuz lortzen diren kurbei kromatograma deitzen zaie.
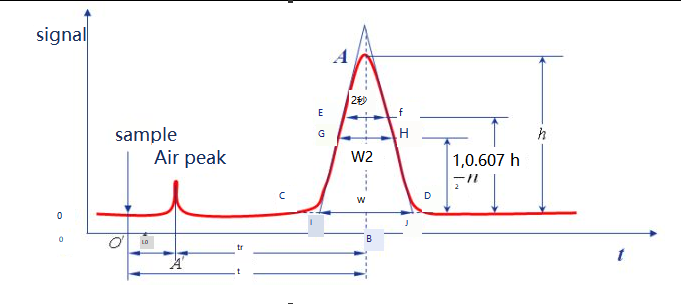
Oinarrizko lerroa:Baldintza kromatografiko jakin batzuetan, fase mugikorra bakarrik detektagailutik pasatzen denean sortzen den seinalearen kurbari oinarrizko lerroa deitzen zaio, ot lerroan agertzen den moduan.Baldintza esperimentala egonkorra zenean, oinarri-lerroa ardatz horizontalarekiko paraleloa zen.Oinarrizko lerroak denboran zehar tresnaren zarata islatzen du, batez ere detektagailuarena.
Gailurraren altuera:puntu gailur kromatografikoaren eta oinarri-lerroaren arteko distantzia bertikala, hz adierazita, AB 'lerroan agertzen den moduan.
Eskualdearen zabalera:Gailu kromatografikoaren eskualde-zabalera bereizketa-eraginkortasunarekin zuzenean lotuta dago.Gailurren zabalera kromatografikoa deskribatzeko hiru metodo daude: σ desbideratze estandarra, W gailurraren zabalera eta FWHM W1/2.
Desbideratze estandarra (σ):σ banaketa normalaren kurbako bi inflexio-puntuen arteko distantzia erdia da, eta σ-ren balioak osagaien sakabanaketa-maila adierazten du zutabetik urrun.Zenbat eta handiagoa izan σ-ren balioa, orduan eta sakabanatuagoak izango dira isuri-osagaiak, eta okerragoa da bereizketa-efektua.Aitzitik, efluenteen osagaiak kontzentratuta daude eta bereizketa-efektua ona da.
Gailurraren zabalera W:Tontor kromatografikoaren bi aldeetako ebakidura-puntuak zuzen ukitzaile gisa erabiltzen dira, eta oinarri-lerroaren ebakidurari gailurraren zabalera edo oinarri-lerroaren zabalera deitzen zaio, eta hori ere W gisa adieraz daiteke, IJ irudian ikusten den bezala.Banaketa normalaren printzipioaren arabera, zabalera gailurraren eta desbideratze estandarraren arteko erlazioa W=4σ dela froga daiteke.
W1/2:Tontorren altueraren erdian dagoen gailurraren zabalera FWHM deitzen da, GHren distantziarako erakusten den moduan.W1/2=2,355σ, W=1,699W1/2.
W1/2, W biak σ-tik eratorritakoak dira eta zutabearen efektua neurtzeaz gain gailur-eremuak kalkulatzeko erabiltzen dira.FWHM neurketa erosoagoa eta erabiliena da.
laburpen laburra
Gailuko irteera-kurba kromatografikotik, helburu hauek lor daitezke:
a, Azterketa kualitatiboa gailur kromatografikoen atxikipen-balioan oinarrituta egin da
b, gailu kromatografikoaren eremuan edo gailurrean oinarritutako analisi kuantitatiboa
C. Zutabearen bereizketa-eraginkortasuna gailur kromatografikoaren atxikipen-balioaren eta gailurraren zabaleraren arabera ebaluatu zen.
Kromatografian parte hartzen duen kalkulu-formula
1. Atxikipen balioa
Atxikipen-balioa zutabean lagin-osagai bat zenbateraino atxikitzen den deskribatzeko erabiltzen den parametro bat da eta karakterizazio kromatografikoaren adierazle gisa erabiltzen da.Bere irudikapen metodoa honakoa da:
Atxikipen-denbora tR
Heriotzaren orduatM
Doitu tR atxikipen-denbora'=tR-tM
(Fase geldialdian igarotako denbora guztira)
Atxikipen bolumena
VR=tR*F.(fase mugikorraren abiaduraren independentea)
Bolumen hila
VM=tM*Fc
(Fase geldikoak okupatzen ez duen espazioa injektoretik detektagailurako fluxu-bidean)
Doitu atxikipen-bolumena VR'=t'R*Fc
2. Atxikipen-balio erlatiboa
Atxikipen-balio erlatiboa, bereizketa-faktorea, zatiketa-koefizientearen ratioa edo gaitasun-faktorea erlatiboa bezala ere ezaguna, probatutako osagaiaren atxikipen-denbora (bolumena) egokituaren eta estandarraren atxikipen-denbora (bolumena) egokituaren erlazioa da baldintza kromatografiko jakin batzuetan.

Atxikipen-balio erlatiboak erabili ziren funtzionamendu-baldintza jakin batzuen eragina ezabatzeko, hala nola emari-abiadura eta finkatzaile-galera, atxikipen-balioetan.Atxikipen-balio erlatiboaren estandarra probatutako laginaren osagai bat edo artifizialki gehitutako konposatu bat izan daiteke.
3. Atxikipen indizea
Atxikipen-indizea X disoluzio finko batean probatu beharreko i substantziaren atxikipen-indizea da. Erreferentziazko substantzia gisa bi n-alano aukeratzen dira, horietako bat N karbono-zenbakia eta besteak N+n.Haien atxikipen-denbora egokitua t 'r (N) eta t 'r (N+n) da, hurrenez hurren, probatu nahi den i substantziaren t 'r (i) atxikipen-denbora doitutakoa haien artean zehazki, hau da, t 'r (N).
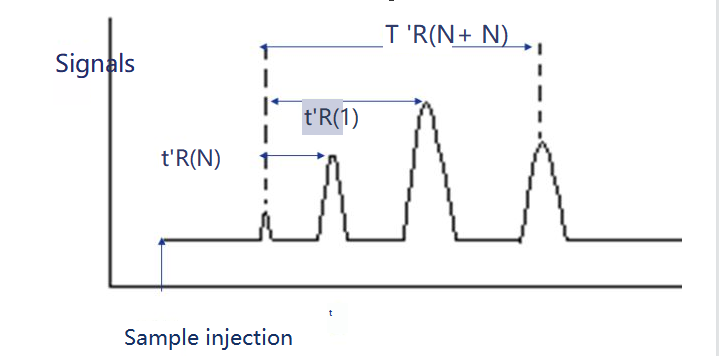
Atxikipen indizea honela kalkula daiteke.
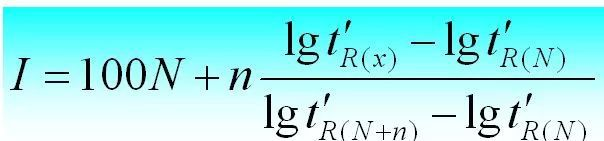
4. Ahalmen-faktorea (k)
Orekan, fase geldikorrean (s) osagai baten masaren eta fase mugikorrean (m) arteko erlazioa, gaitasun-faktorea deritzona.Formula hau da:
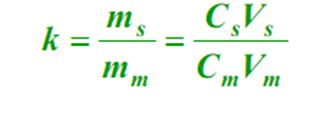
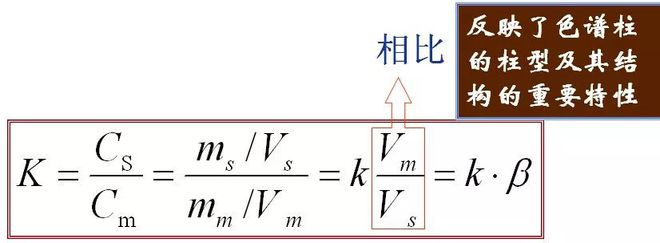
5、Partizio-koefizientea (K) Orekan, fase geldikorrean (s) osagai baten kontzentrazioa eta fase mugikorrean (m) arteko erlazioa, zatiketa-koefizientea deritzona.Formula hau da

K eta k arteko erlazioa:
Zutabe mota eta bere korapiloaren egituraren propietate garrantzitsuak islatzen ditu
laburpen laburra
Atxikipen-balioaren eta gaitasun-faktorearen eta zatiketa-koefizientearen arteko erlazioa:
Banaketa kromatografikoa lagin erlatibo finko batean osagai bakoitzaren adsortzio- edo disoluzio-ahalmenaren diferentzian oinarritzen da, eta zatiketa-koefizientearen K (edo gaitasun-faktorearen k) balioaren tamainaren arabera adieraz daiteke kuantitatiboki.
Adsortzio edo disoluzio gaitasun handia duten osagaiek zatiketa koefiziente handia (edo gaitasun-faktorea) eta atxikipen denbora luzea dute.Aitzitik, adsortzio edo disolbagarritasun ahula duten osagaiek zatiketa koefiziente txikia eta atxikipen denbora laburra dute.
Kromatografiaren oinarrizko teoria
1. Erretiluen teoria
(1) Aurkeztu -- teoria termodinamikoa
Martinek eta Syngek proposatutako dorre plaka ereduarekin hasi zen.
Zatiketa-zutabea: erretiluan gas-likido orekako hainbat aldiz, bereizketa ezberdinen irakite-puntuaren arabera.
Zutabea: osagaiak bi faseen arteko zatiketa anitzen bidez orekatzen dira eta zatiketa koefiziente ezberdinen arabera bereizten dira.
(2) Hipotesia
(1) Zutabean erretilu asko daude, eta osagaiak azkar irits daitezke banaketa orekara erretiluaren tartean (hau da, erretiluaren altuera).
(2) Fase mugikorra zutabean sartzen da, ez jarraian baina taupadaka, hau da, pasabide bakoitza zutabe bolumen bat da.
(3) Lagina zutabe-plaka bakoitzari gehitzen zitzaionean, laginaren difusioa zutabearen ardatzean zehar baztertu liteke.
(4) Banaketa-koefizientea erretilu guztietan berdina da, osagai kopuruaren arabera.Hau da, zatiketa koefizientea konstantea da taban bakoitzean.
(3) Printzipioa
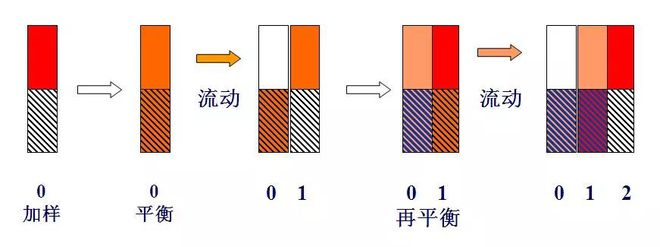
Erretiluen teoriaren diagrama eskematikoa
Masa-unitateko osagai bat, hots, m=1 (adibidez, 1mg edo 1μg), 0 zenbakiko erretiluari gehitzen bazaio, eta banaketa-oreka egin ondoren, k=1, hots, ns=nm, nm=ns=0,5.
Gas eramailearen plaka-bolumen bat (lΔV) 0 plaka pultsazio moduan sartzen denean, gas fasean nm osagaia duen gas eramailea 1. plakara bultzatzen da. Une honetan, 0 plakaren fase likidoko ns osagaia. eta 1. plakaren gas faseko nm osagaia bi faseen artean banatuko da.Beraz, 0 plakan jasotako osagaien guztizko kopurua 0,5 da, zeinetan fase gaseosoa eta likidoa 0,25 bakoitza, eta 1. plakan jasotako kopuru osoa ere 0,5 da.Gas eta likido faseak ere 0,25 izan ziren.
Prozesu hau errepikatzen da plaka-bolumen-gas eramaile berri bat zutabean pultsatzen den bakoitzean (ikus beheko taula).
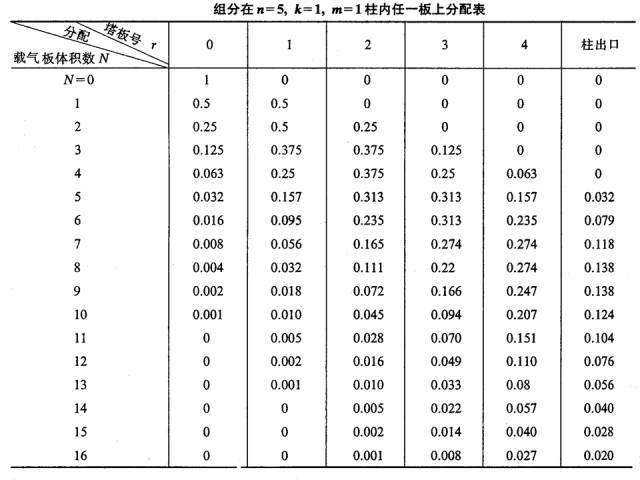
(4)Kromatografiko irteera-kurba ekuazioa

σ desbideratze estandarra da, atxikipen-denbora da, C edozein unetan dagoen kontzentrazioa da,
C, injekzio-kontzentrazioa da, hau da, osagaien kopuru osoa (A gailurraren eremua).
(5) zutabearen eraginkortasun parametroak
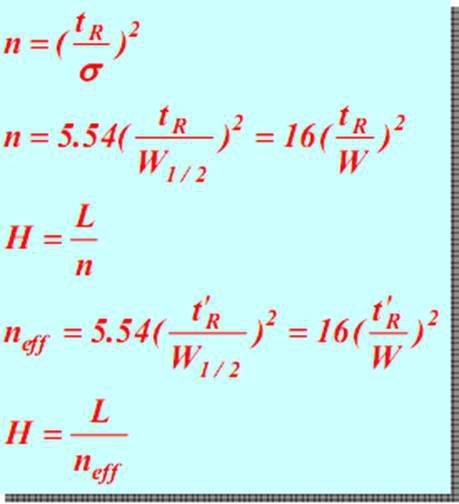
tR konstantean, zenbat eta W edo w 1/2 txikiagoa (hau da, orduan eta gailur estuagoa), orduan eta handiagoa da n plaka teoriko kopurua, orduan eta txikiagoa da plaka teorikoa altuera eta orduan eta handiagoa da zutabearen bereizketa-eraginkortasuna.Gauza bera gertatzen da teoria eraginkorra neff erretiluarekin.Beraz, erretiluen kopuru teorikoa zutabeen eraginkortasuna ebaluatzeko indizea da.
(5)Ezaugarriak eta gabeziak
> Abantailak
Erretiluaren teoria erdi-enpirikoa da eta irteera-kurbaren forma azaltzen du
Osagaien zatiketa eta bereizketa prozesuak azaltzen dira
Zutabearen eraginkortasuna ebaluatzeko indize bat proposatzen da
> Mugak
Osagaiak ezin dira benetan banaketa orekara iritsi bi faseetan:
Ezin da zutabeko osagaien hedapen longitudinala alde batera utzi:
Ez zen kontuan hartu hainbat faktore zinetikok masa-transferentzia prozesuan duten eragina.
Zutabe-efektuaren eta fase mugikorraren fluxu-abiaduraren arteko erlazioa ezin da azaldu:
Ez dago argi zein faktore nagusiek eragiten duten zutabearen eragina
Problema hauek tasaren teorian behar bezala ebazten dira.
2. Tasa-teoria
1956an, VanDeemter et al.erretiluaren teoriaren kontzeptua xurgatu zuen, eta erretiluaren altueran eragiten duten faktore zinetikoak konbinatu zituen, prozesu kromatografikoaren teoria zinetikoa aurkeztu zuen - tasa teoria eta VanDeemter ekuazioa eratorri zuen.Prozesu kromatografikoa orekarik gabeko prozesu dinamikotzat hartzen du eta faktore zinetikoek gailurraren zabalkuntzan duten eragina aztertzen du (hau da, zutabe-efektua).
Geroago, Giddings eta Snyder et al.kromatografia likidoaren tasaren ekuazioa (Giddings ekuazioa alegia) proposatu zuen VanDeemter ekuazioan oinarrituta (gero gas kromatografia tasaren ekuazioa deitua) eta likidoaren eta gasaren arteko propietate-diferentziaren arabera.
(1) Van Deemter ekuazioa
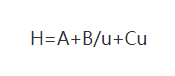
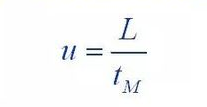
Non: H: taularen altuera da
A: zurrunbiloaren difusio-terminoaren koefizientea
B: difusio molekularren terminoaren koefizientea
C: masa transferitzeko erresistentzia terminoaren koefizientea
(2) Giddings ekuazioa
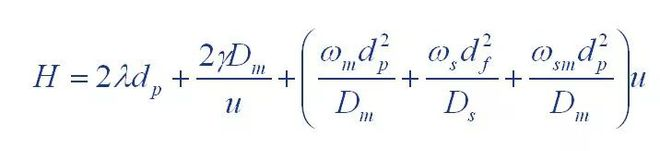
Azterketa kuantitatiboa eta kualitatiboa
(1) Analisi kualitatiboa
Analisi kromatografiko kualitatiboa gailur kromatografiko bakoitzak adierazten dituen konposatuak zehaztea da.Hainbat substantziak baldintza kromatografiko jakin batzuetan atxikipen-balio zehatzak dituztenez, atxikipen-balioa indize kualitatibo gisa erabil daiteke.Gaur egun, hainbat metodo kualitatibo kromatografiko atxikipen-balioetan oinarritzen dira.
Hala ere, substantzia ezberdinek baldintza kromatografiko berdinetan atxikipen-balio antzekoak edo berdinak izan ditzakete, hau da, atxikipen-balioak ez dira esklusiboak.Beraz, zaila da guztiz ezezaguna den lagin bat atxikipen-balioetan soilik oinarrituta karakterizatzea.Laginaren iturria, izaera eta helburua ulertuta, laginaren konposizioaren aurretiazko epaiketa egin daiteke, eta honako metodo hauek erabil daitezke gailur kromatografikoak adierazten duen konposatua zehazteko.
1. Kontrol kualitatiboa substantzia puruak erabiliz
Baldintza kromatografiko jakin batzuetan, ezezagun batek atxikipen-denbora definitua baino ez du.Beraz, ezezaguna kualitatiboki identifikatu daiteke, baldintza kromatografiko berdinetan ezagutzen den substantzia puruaren atxikipen denbora substantzia ezezagunaren atxikipen denborarekin alderatuz.Biak berdinak badira, substantzia ezezaguna substantzia puru ezagun bat izan daiteke;Bestela, ezezaguna ez da substantzia purua.
Substantzia puruen kontrol-metodoa bere konposizioa ezagutu den, konposizio nahiko sinplea den eta substantzia purua ezagutzen duen substantzia ezezagunari soilik aplikatzen zaio.
2. Atxikipen-balio erlatiboaren metodoa
α atxikipen-balio erlatiboa, i osagaiaren eta erreferentziazko materialen arteko doikuntzari egiten dio erreferentzia Atxikipen-balioen ratioa:
Finkatzailearen eta zutabearen tenperaturaren aldaketarekin bakarrik aldatzen da, eta ez du zerikusirik beste funtzionamendu-baldintzekin.
Geldiko fase eta zutabe-tenperatura jakin batean, i osagaiaren eta erreferentziazko substantziaren s erretentzio-balioak hurrenez hurren neurtzen dira, eta, ondoren, goiko formularen arabera kalkulatzen dira.Lortutako atxikipen-balio erlatiboak literaturan dagozkien balioekin kualitatiboki aldera daitezke.
3, substantzia ezagunak gehituz altuera gailurraren metodoa handitzeko
Lagin ezezagunean osagai asko daudenean, lortutako gailur kromatografikoak trinkoegiak dira goiko metodoarekin erraz identifikatu ahal izateko, edo lagin ezezaguna zehaztutako elementuen analisirako soilik erabiltzen denean.
«Lehenengo lagin ezezagun baten kromatograma egiten da, eta gero kromatograma gehiago lortzen da lagin ezezagunari substantzia ezagun bat gehituz».Gailur altuera handitu duten osagaiak ezagutu daitezke substantzia horietarako.
4. Mantendu indizearen metodo kualitatiboa
Atxikipen-indizeak finkatzaileetan substantzien atxikipen-jokaera adierazten du eta gaur egun GC-n gehien erabiltzen den eta nazioartean aitortzen den indize kualitatiboa da.Erreproduzigarritasun ona, estandar uniformea eta tenperatura koefiziente txikiaren abantailak ditu.
Atxikipen-indizea fase geldikorraren eta zutabearen tenperaturaren propietateekin soilik dago lotuta, baina ez beste baldintza esperimentalekin.Bere zehaztasuna eta errepikakortasuna bikainak dira.Zutabearen tenperatura fase geldikoaren berdina den bitartean, literatura-balioa aplika daiteke identifikaziorako, eta ez da beharrezkoa material purua konparatzeko erabiltzea.
(2)Analisi kuantitatiboa
Kuantifikazio kromatografikoaren oinarriak:
Analisi kuantitatiboaren zeregina lagin mistoan ehun osagai aurkitzea da
Zatikako edukia.Kuantifikazio kromatografikoa honako hauetan oinarritzen zen: funtzionamendu-baldintzak koherenteak zirenean, zen
Neurtutako osagaiaren masa (edo kontzentrazioa) detektagailuak emandako erantzun seinalearen arabera zehazten da
Proportzionala da.Alegia:
Kuantifikazio kromatografikoaren oinarriak:
Analisi kuantitatiboaren zeregina lagin mistoan ehun osagai aurkitzea da
Zatikako edukia.Kuantifikazio kromatografikoa honako hauetan oinarritzen zen: funtzionamendu-baldintzak koherenteak zirenean, zen
Neurtutako osagaiaren masa (edo kontzentrazioa) detektagailuak emandako erantzun seinalearen arabera zehazten da
Proportzionala da.Alegia:
1. Gailur eremua neurtzeko metodoa
Peak area kromatogramek emandako oinarrizko datu kuantitatiboak dira, eta gailur eremuaren neurketaren zehaztasunak zuzenean eragiten die emaitza kuantitatiboei.Neurketa-metodo desberdinak erabili ziren gailur kromatografikoetarako gailur forma desberdinak zituzten.
Zaila da neguaren balio zehatza aurkitzea analisi kuantitatiboan:
Alde batetik injekzio bolumen absolutua zehaztasunez neurtzeko zailtasunagatik: bestetik
Gailur-eremua baldintza kromatografikoen menpe dago, eta banda kromatografikoa mantendu behar da balioa neurtzean.
Ez da posible ezta komenigarria gauza bera egitea.Eta ondo atera dezakezun arren
Balio zehatza, gainera, estandar bateraturik ez dagoelako eta ezin delako zuzenean aplikatu.
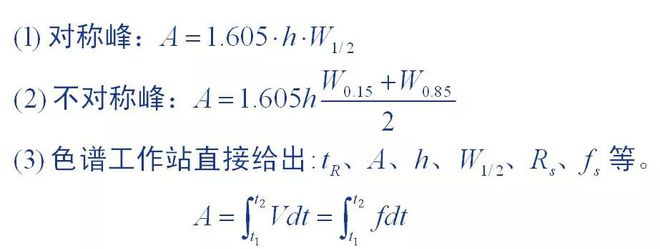
2.Zuzenketa-faktore kuantitatiboa
Zuzenketa-faktore kuantitatiboaren definizioa: detektagailura sartzen diren osagaien kopurua (m)
Bere gailurraren eremu kromatografikoaren (A) edo gailurraren altueraren () proportzionaltasun-konstante bat da (,
Proportzionaltasun-konstanteari osagaiaren zuzenketa-faktore absolutua deitzen zaio.
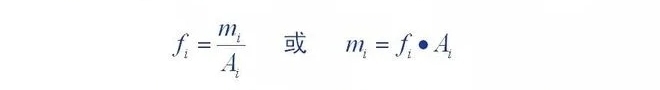
Zaila da neguaren balio zehatza aurkitzea analisi kuantitatiboan:
Alde batetik injekzio bolumen absolutua zehaztasunez neurtzeko zailtasunagatik: bestetik
Gailur-eremua baldintza kromatografikoen menpe dago, eta banda kromatografikoa mantendu behar da balioa neurtzean.
Ez da posible ezta komenigarria gauza bera egitea.Eta ondo atera dezakezun arren
Balio zehatza, gainera, estandar bateraturik ez dagoelako eta ezin delako zuzenean aplikatu.
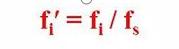
Hau da, osagai baten zuzenketa-faktore erlatiboa osagaia eta erreferentzia-materiala da
Zuzenketa-faktore absolutuen ratioa.
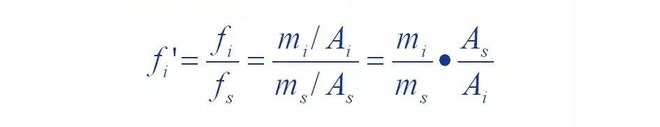
Ikusten da zuzenketa-faktore erlatiboa osagaiaren kalitatea estandarraren aldean dagoenean.
Substantzia s berdina denean, erreferentzia-materialaren gailurraren azalera osagaiaren gailurraren azalera da
Anitz.Osagairen batek m masa eta A gailur eremua baditu, orduan f'A kopurua
Balioak masa duen erreferentzia-materialaren gailurraren azaleraren berdinak dira.Beste hitz batzutan,
Zuzenketa-faktore erlatiboaren bidez, osagai bakoitzaren gailur-eremuak bereiz daitezke
Erreferentzia-materialaren gailur-eremua bere masaren berdina bihurtu da, gero erlazioa
Estandarra bateratua dago.Beraz, osagai bakoitzaren ehunekoa kalkulatzeko metodo normalizatua da
Kantitatearen oinarria.
Zuzenketa-faktore erlatiboa lortzeko metodoa: zuzenketa-faktore erlatiboaren balioak izatearekin soilik alderatu dira
Neurketa estandarrari eta detektagailu motari dagokio, baina funtzionamendu-bandarekin
Berdin du.Beraz, literaturako erreferentzietatik atera daitezke balioak.Testua bada
Eskaintzan nahi duzun balioa aurkitzen ez baduzu, zuk zeuk ere zehaztu dezakezu.Determinatzeko metodoa
Metodoa: neurtutako substantziaren kopuru jakin bat hautatutako hamar erreferentziazko material → kontzentrazio jakin batean bihurtu
Bi osagaietako gailur kromatografikoak A eta As neurtu dira.
Hori da formula.
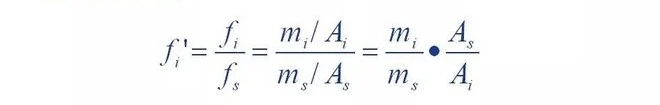
3. Kalkulu kuantitatiboaren metodoa
(1) Eremua normalizatzeko metodoa
Pikorik gabeko frakzio guztien edukiaren batura % 100 gisa kalkulatu zen kuantifikaziorako
Metodoari normalizazioa deitzen zaio.Bere kalkulu-formula hau da:
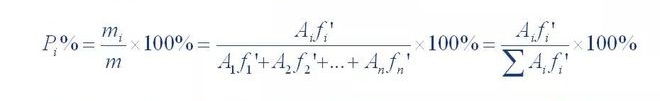
Non P,% probatutako osagaien ehunekoa den;A1, A2... A n 1 osagaia da.1~n-ren gailurraren azalera;f'1, f'2... f'n 1etik n osagaietarako zuzenketa-faktore erlatiboa da.
(2) kanpoko metodo estandarra
Laginean probatu beharreko osagaiaren erantzun-seinalearen eta kontrol gisa probatu beharreko osagai hutsaren arteko konparazio kuantitatiboaren metodoa.
(3) Barne-metodo estandarra
Barne-metodo estandarra deitzen den metodoa da, substantzia puru kopuru jakin bat probatutako substantziaren disoluzio estandarrari eta lagin-soluzioa barne-estandar gisa gehitzen zaiona, eta, ondoren, aztertu eta zehazten da.
(3) gehiketa metodo estandarra
Gehitze-metodo estandarra, barne-gehitze-metodo bezala ere ezaguna, (△C) kopuru jakin bat gehitzea da.
Saiakuntzako substantziaren erreferentzia probatu beharreko lagin-disoluzioari gehitu zitzaion, eta proba entseguari gehitu zitzaion
Substantziaren ondoren lagin-disoluzioaren gailurra jatorrizko lagin-disoluzioarena baino handiagoa izan zen
Eremuaren gehikuntza (△A) erabili zen lagin-disoluzioko substantziaren kontzentrazioa kalkulatzeko
Edukia (Cx)
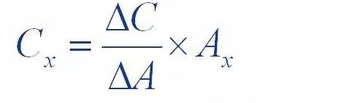
Non Ax jatorrizko laginean neurtu beharreko substantziaren gailurraren azalera den.

Argitalpenaren ordua: 2023-mar-27